Ao longo dos tempos, os cientistas foram alterando a forma do átomo consoante as suas descobertas pois a ciência ao progredir deu essa possibilidade, de conseguirem executar experiências e delas tirarem as suas conclusões.
Modelo Atómico de Dalton:
No início do séc. XIX, o cientista John Dalton com base no que se pensava naquele tempo, concluiu que o átomo era um corpúsculo esférico, indivisível e indestrutível.
 |
| John Dalton |
 |
| Modelo Atómico de Dalton |
Modelo Atómico de Thomson:
Nos finais do século XIX, o cientista Joseph Thomson tirou novas conclusões acerca do modelo atómico. Através de uma experiência de tubos de descarga, Thomson verificou que o átomo tinha partículas de carga elétrica negativa, designadas de eletrões. Assim, Thomson pôde concluir que os átomos eram corpúsculos de carga elétrica positiva, onde se encontravam espalhados os eletrões, com carga negativa, fazendo com que a carga total do átomo ficasse nula. Surgiu assim o primeiro modelo de átomo divisível.
 |
| Joseph Thomson |
 |
| Modelo Atómico de Thomson |
Modelo Atómico de Rutherford:
No início do século XX, o cientista neozelandês Ernest Rutherford, após várias experiências com partículas
 |
| Ernest Rutherford |
α pode concluir que:
 |
| Modelo Atómico de Rutherford |
- A maior parte do átomo era espaço vazio;
- O átomo tinha um núcleo pequeno de carga elétrica positiva, onde se concentrava toda a massa do átomo;
- Os eletrões, com carga elétrica negativa, moviam-se à volta do núcleo, como os planetas se movem em volta do Sol.
Assim surgiu o primeiro modelo planetário do átomo.
Modelo Atómico de Bohr:
Pouco tempo depois, Niels Bohr completou o modelo atómico do cientista neozelandês com as suas ideias:
- Os eletrões movem-se à volta do núcleo com as suas órbitas circulares;
- Os eletrões com mais valor de energia movem-se em órbitas mais afastadas do núcleo, enquanto os que têm menos valor de energia movem-se em órbitas mais próximas do núcleo.
 |
| Niels Bohr |
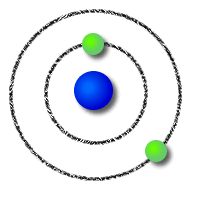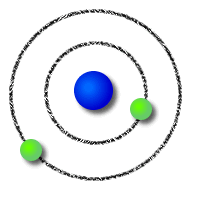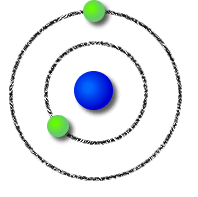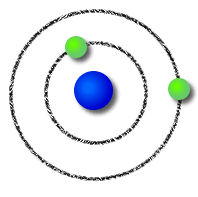 |
| Modelo Atómico de Bohr |
Sem comentários:
Enviar um comentário